Ocena skuteczności sondy FlexISH ALK / ROS1 DistinguISH ™
Rak płuc jest główną przyczyną śmiertelności związanej z zachorowalnością na nowotwory, która wynosi około 1,6 mln zgonów rocznie na całym świecie. Odpowiada za około 19% wszystkich zgonów związanych z nowotworami.
Według wytycznych: College of American Pathologists (CAP) oraz International Association for the Study of Lung Cancer (IASLC) a także Association for Molecular Pathology (AMP) diagnostyka w kierunku aberracji EGFR i ALK powinna dotyczyć wszystkich badanych gruczolakoraków (adenocarcinoma) w tym także tych związanych z nowotworami płuc, niezależnie od czynników takich jak wiek, płeć pacjenta, czy palenie papierosów.
Badania kliniczne wykazują, iż całkowite przeżycie pacjentów z translokacją ALK leczonych kryzotynibem lub pacjentów z mutacją EGFR leczonych inhibitorami EGFR, takimi jak gefitynib lub erlotynib było znacząco wydłużone w porównaniu z pacjentami leczonymi standardową chemioterapią. Podobnie biomarkery- rearanżacje w obrębie genów ROS1 lub RET, mają obiecujący potencjał w odniesieniu do stosowania terapii celowanej.
Niedawno przeprowadzone testy dotyczą skuteczności sondy FlexISH® ALK / ROS1 DistinguISH ™ przy pomocy technik FISH w nie drobnokomórkowym raku płuca
Przeprowadzona analiza pozwoliła na porównanie wydajności multipleksowego testu FISH z użyciem sondy FlexISH® ALK / ROS1 DistinguISH ™ względem badań wykonywanych przy użyciu pojedynczych sond pozwalających na ocenę aranżacji w obrębie genów ALK i ROS1. Wykonane testy miały na celu przedstawienie możliwości diagnostycznych, pozwalających na zminimalizowanie niepotrzebnego zużycia większego fragmentu badanej tkanki w czasie procesu diagnostycznego, poprzez wykonanie jednego testu w kierunku zróżnicowania rearanżacji w obrębie genów ALK i ROS1, przy jednoczesnym rozróżnieniu między możliwymi aberracjami wpływającymi na oba regiony chromosomalne.
W teście wykorzystana została sonda FlexISH® ALK / ROS1 DistinguISH™ (producent: Zytovision, Bremerhaven, Niemcy). Badanie przeprowadzone zostało na zestawie 28 próbek nowotworów o znanym statusie genu ALK i ROS1.
Sonda FlexISH® ALK / ROS1 DistinguISH™ przeznaczona jest do wykrywania rearanżacji w obrębie genu ALK (tyrozynowy receptor chłoniaka anaplastycznego) i ROS1 (c-ros onkogenu 1). Korzystając z tej sondy, możliwe jest jednoczesne wykrywanie rearanżacji genu ALK i ROS1, oraz dodatkowo, rozróżnienie między możliwymi aberracjami wpływającymi na oba regiony chromosomalne.
Zarówno gen ALK, jak i ROS1 kodują białka transbłonowej receptorowej kinazy tyrozynowej. Przegrupowania wpływające na locus genu ALK lub ROS1 często występują w niedrobnokomórkowym raku płuca (NSCLC).
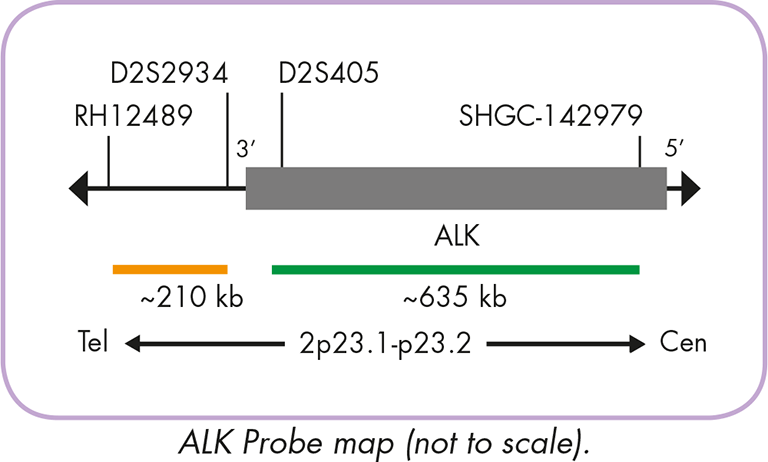
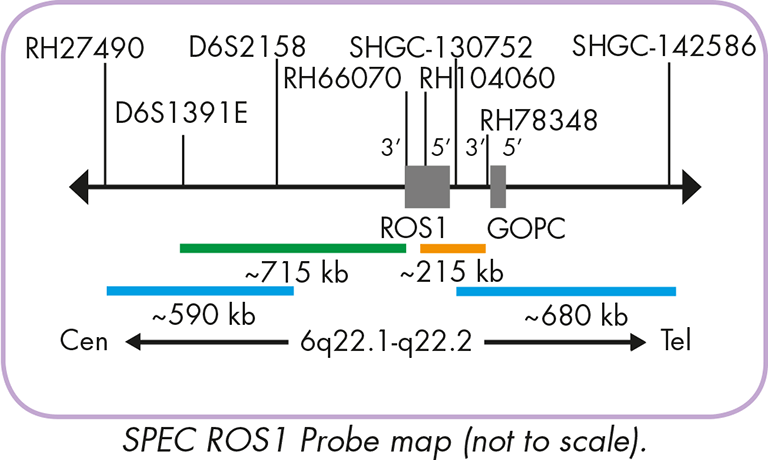
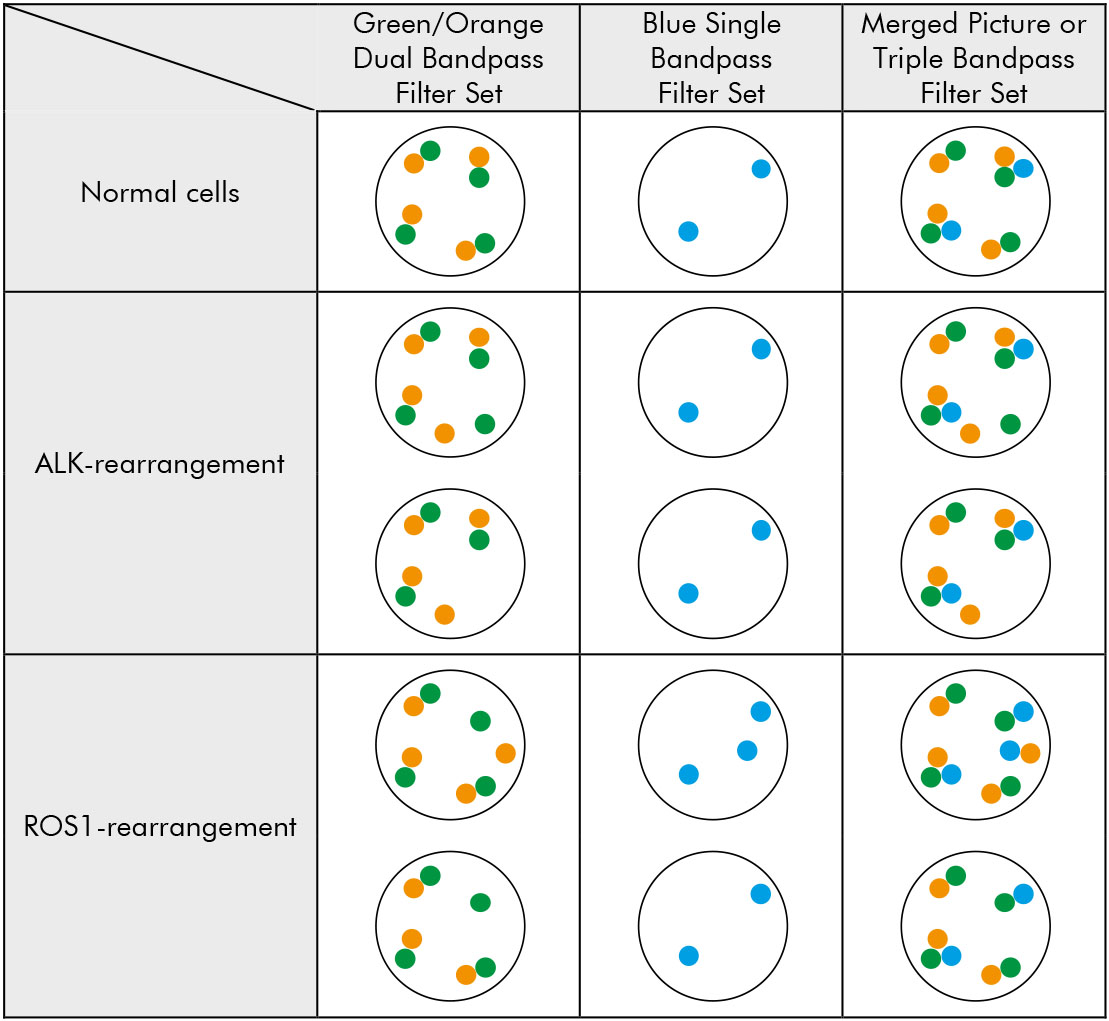
Oczekiwane wyniki w normalnych i podlegających rearanżacji jądrach interfazowych
Wyniki testu przeprowadzonego z użyciem sondy FlexISH® ALK / ROS1 DistinguISH™ były w 100% zgodne z wynikami uzyskanymi w oparciu o rutynowo stosowane sondy pojedyncze - ALK i ROS1 (15 rearanżacji typu ALK i 3 rearanżacje typu ROS1). W teście nie zaobserwowano żadnych wyników fałszywie pozytywnych.
Przeprowadzone badanie wykazało, iż sonda FlexISH® ALK / ROS1 DistinguISH™ jest istotnym odczynnikiem pozwalającym na jednoczesną ukierunkowaną diagnostykę w kierunku rozróżnienia rearanżacji w obrębie genów ALK i ROS1. Przekłada się to na oszczędność materiału diagnostycznego, który może zostać wykorzystany do innych badań diagnostycznych.
Sonda FlexISH® ALK / ROS1 DistinguISH™ dostępna jest w naszej ofercie pod następującymi numerami katalogowymi:
- ZV-Z-2203-50 - odczynnik pozwalający na wykonanie 5 testów
- ZV-Z-2203-200- odczynnik pozwalający na wykonanie 20 testów
Niniejszy odczynnik przeznaczony jest do diagnostyki In Vitro.
Piśmiennictwo:
- Evaluation of a Dual ALK/ROS1 Fluorescent In Situ Hybridization Test in Non–Small-cell Lung Cancer - Florent Ginestet1, Laetitia Lambros1, Glen Le Flahec1, Pascale Marcorelles1, Arnaud Uguen- Clin Lung Cancer 2018; 19: e647-e653
- Strona producenta: www.zytovision.com
- „Kryzotynib — nowy lek ukierunkowany molekularnie w leczeniu nie drobnokomórkowego raka płuca” Rafał Czyżykowski, Sylwia Dębska, Maja Habib, Magdalena Krakowska, Joanna Kubicka, Piotr Potemski Klinika Chemioterapii Nowotworów, Katedra Onkologii Uniwersytetu Medycznego w Łodzi, Szpital im. Mikołaja Kopernika w Łodzi- Onkologia w Praktyce Klinicznej 2012, tom 8, nr 5, 197–203 Copyright © 2012 Via Medica ISSN 1734–3542 www.opk.viamedica.pl